의료기기 안전 활용 위한 ‘적합성 평가’의 중요성

▲양 미 숙
국립전파연구원 정보통신적합성평가과 사무관
ICT 기술 환경 변화와 적합성평가
AI 기반 디지털 전환으로 인해 정보통신기술(ICT) 환경은 급변하게 변화하고 있다. 이런 변화는 사회의 생활 방식은 물론 제조·생산 산업과 유통구조까지 빠르게 바꾸고 있다. 이에 따라 의료기기를 포함해 저궤도위성 단말 등 다양한 방송통신기기가 시장에 출시되고 있다. 이런 제품들은 기술적 안전성과 전자파 혼·간섭 방지 문제가 동반되므로, 국민의 생명과 재산 보호를 위해 더욱 중요하게 인식돼야 한다.
특히 의료분야에서는 인공와우, 보청기, 심장박동기 등과 같은 체내이식형 무선기기와 5G 기반 스마트 의료서비스 등에도 전파 기술이 활용되고 있다. 의료기기는 단순한 치료 목적을 넘어 ICT와 결합한 의료·통신 융복합 기기로 발전하고 있다.
우리나라는 이런 방송통신기자재 등에 대해 제조·수입·판매 이전에 시험·평가를 통한 사전규제 방식의 적합성평가 제도를 시행하고 있다.
미국, 일본 등 주요 국가들 역시 자국 내에서 유사한 제도를 운영하고 있으며, 다자간 협정을 통해 상호 절차를 인정하는 등 국제적 협력도 확대되고 있다.
본 기고는 의료기기 산업계가 적합성평가 제도에 대한 이해를 높이고, 관련 규정을 준수하는 데 도움을 주고자 한다. 아울러 의료기기 신제품 개발 및 빠른 시장 출시를 위한 정부와의 소통 방안도 함께 제시하고자 한다.
방송통신기자재 등의 적합성평가 개요
적합성평가는 방송통신기자재 등의 안전한 전파 이용 환경과 국민의 안전을 보장하기 위한 제도이다. 방송통신기자재 등을 제조·수입·판매하기 전에 해당 기기가 기술기준에 적합한지를 시험해 △적합인증 △적합등록 △자기적합확인 △잠정인증을 받는 절차이다.
적합성평가의 법적 근거는 ‘전파법’ 제58조의2에 명시돼 있으며, 평가 유형은 전자파 위해도의 경중에 따라 구분된다.
전자파 위해도가 높은 제품은 ‘적합인증’을 받아야 하며, 적합인증의 대상이 아닌 경우 ‘적합등록’ 대상으로 분류된다. 전파 환경 및 방송통신망 등에 미치는 위해가 낮은 기기는 지난해 7월 도입된 ‘자기적합확인’ 대상이 된다. 기술기준이 없거나 시험이 곤란한 경우에는 ‘잠정인증’ 방식으로 평가가 이뤄진다.
적합성평가를 통과한 제품은 ‘방송통신기자재등의 적합성평가에 관한 고시’ 제26조 별표5에 따라 적합성평가번호 등을 포함한 KC마크를 표시해야 한다. 표시 방법은 부착 외에도 QR코드 등을 활용한 전자적 정보 제공 방식(e-labelling)도 가능하다.
시험은 ‘전파법’ 제58조의5에 따라 국립전파연구원장이 지정한 시험기관에서 실시한다. 자기적합확인 대상 기기의 경우, 자체 시험 능력이 있는 기업은 자가 시험이 가능하다.
지정시험기관은 분야에 대한 인력, 설비, 국제표준(ISO/IEC 17025)에 적합한 품질관리규정 준수 여부 등에 대한 심사를 통과해야 지정될 수 있다.
의료기기 적용 기술기준과 시험 절차
적합성평가에 적용되는 기술기준은 제품의 특성에 따라 유선, 무선, 전자파 인체보호 세 분야로 나뉜다.
유선 분야는 ‘방송통신발전 기본법’ 제28조 및 ‘인터넷 멀티미디어 방송사업법’ 제14조의2를, 무선 분야는 ‘전파법’ 제45조 및 제47조의2를 따른다. 전자파 인체보호는 ‘전파법’ 제47조의2에 따른 전자파흡수율(SAR) 측정 기준 또는 전자파 강도 측정 기준을 적용한다.
이와 별개로 모든 분야에는 공통으로 ‘전자파적합성 기준’(EMC)을 적용한다. 의료기기는 해당 기준 제6조 별표3의2에 따라 ‘KS C IEC 60601-1-2:2012’ 시험방법을 적용받는다.
유선, 무선 또는 인체보호에 해당하는 경우, 각각의 분야에 맞는 시험을 모두 거쳐 적합성평가를 받아야 한다. 적합성평가를 받은 제품이 적합성평가 당시에서 변경사항이 발생한 경우 신규로 적합성평가를 받아야 하나, 제도 간소화를 위해 기술기준 관련 사항과 유지·관리에 관한 사항으로 구분해 변경신고 절차를 운영한다. 이때 기술기준 관련 변경사항은 적합성평가 시험을 거쳐 시험성적서 등 변경 사실을 증명하는 서류를 제출해야 한다.
적합성평가의 사후관리
사후관리는 적합성평가를 받은 제품이 평가 당시의 성능 및 기술기준을 계속해서 충족하며 제조·유통되고 있는지를 확인하기 위한 제도다. 이는 불량 기기의 유통을 방지하고 소비자를 보호하며 전파 이용 질서를 유지하기 위한 사후규제적 성격을 가진다.
‘전파법’ 제71조의2에 따라 가능한 시중에 유통되는 제품을 직접 구입해 시험하며, 법 위반 사항이 발생한 경우에는 ‘전파법 시행령’ 제118조제2호 별표23에 따라 적합성평가 취소 또는 과태료 등의 행정처분을 내릴 수 있다.
또한, 적합성평가를 받지 않은 불법 기기에 대해서는 중앙전파관리소가 전국 10개 지방지소를 통해 조사 및 단속을 진행하고 있다.
국가 간 적합성평가 상호인정 협정(MRA)
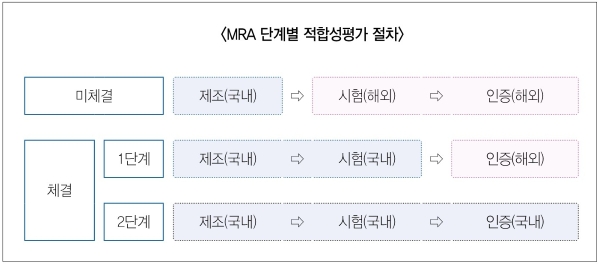
MRA는 ICT 기기의 수출 시 상대국의 기술기준에 따른 적합성평가 시험 또는 인증 결과를 자국에서 수행한 것으로 인정받는 제도이다. 1단계 MRA는 자국에서 실시한 시험을 상대국에서 인정해 주는 방식이며, 2단계는 자국에서 시험을 실시하고 상대국의 인증서까지 자국에서 발급할 수 있도록 허용하는 방식이다. 이는 각국에서 ICT 기기 수출을 보다 쉽고 빠르게 진행하고 시간과 비용 절감을 위한 것으로, 주요국들은 MRA 체결을 지속적으로 희망하고 있다.
우리나라는 현재 미국, 캐나다, EU 등 33개국과 MRA를 체결하고 있으며, 이 중 캐나다와는 2단계 협정을 통해 국내 전파시험인증센터에서 인증서 발급이 가능하다.
결론
국내 방송통신기자재 등의 적합성평가 제도는 1967년 ‘전파관리법’에서 무선기기를 대상으로 시작됐다. 이후 기간통신망 보호를 위한 유선기기 평가, 전자파 이용환경 보호를 위한 전자파적합성으로 점차 영역을 확대해 왔으며, 2011년에 시대 변화에 따라 현재의 적합성평가 체계로 크게 개편됐다. 이제는 5G를 넘어 6G를 위한 ‘초연결’·‘초고속’·‘초융합’의 3초 시대를 이루기 위한 전 세계적 경쟁에 대응하기 위해 적합성평가 제도는 시장 중심으로 변화해야 한다.
의료기기산업은 국내 제조·수입업체들이 산업 기반을 확대하며 외형적으로 성장하고 있다. 앞으로는 외형적 성장뿐 아니라 기술 융합, 응용 분야 확대 등 구조적 변화도 병행될 것으로 예상된다. 이에 새로운 의료기기의 출현을 대비해 정부와 산업계는 새로운 기술기준 마련, 절차 개선 등에서 긴밀하게 협력해야 한다.
http://www.kmdianews.com/news/articleView.html?idxno=66565